Infertilidad, definida como la ausencia de un embarazo después de 1 año de relaciones sexuales sin protección, afecta a 1 de cada 13 parejas en Estados Unidos (1). La infertilidad por factor masculino constituye entre un 25% y un 30% de todos los casos de infertilidad y en combinación con la infertilidad femenina contribuye en otro 30%. Simultáneamente, el recuento de espermatozoides entre los varones occidentales actualmente está disminuyendo (2) con más de 15% parejas incapaces de concebir dentro de un año de relaciones sexuales sin protección, por ahora (3). Entre los casos de infertilidad masculina, un 10% no presentan espermatozoides en el eyaculado, un trastorno conocido como azoospermia. De este modo, un 0.8-1% de todos hombres no tienen espermatozoides en el eyaculado.
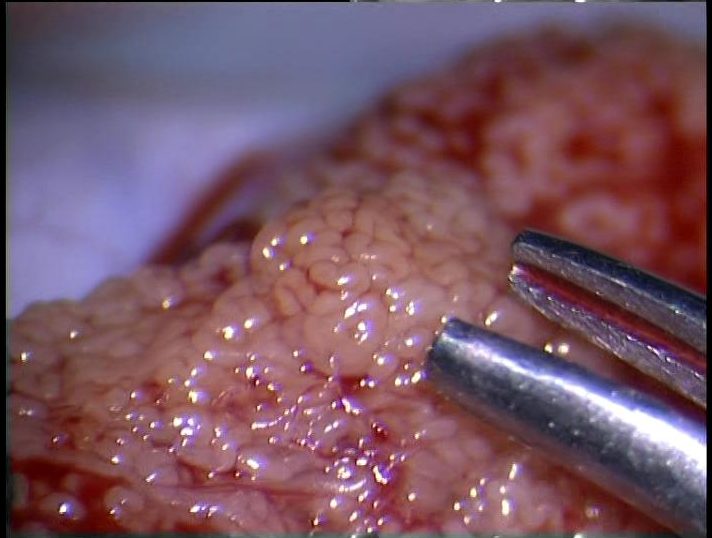
Hay muchas causas, pero con mayor frecuencia ocurre debido a un trastorno llamado bloqueo de espermatogénesis. Se trata de un problema de producción de espermatozoides que consiste en que los hombres o no producen espermatozoides en los testículos o producen muy poco y sólo en pequeñas zonas de los testículos, más que la producción uniforme que se observa en el caso de varones fértiles. Para los hombres con un bloqueo de espermatogénesis, tener hijos significa someterse a un tratamiento importante, con el fin de obtener espermatozoides de los testículos quirúrgicamente. Previo a la cirugía, tendrán que hacer dos análisis de semen en una clínica de fertilidad para confirmar la ausencia de espermatozoides y también tendrán que someterse a una prueba genética con el fin de determinar si tienen uno de los trastornos poco comunes que podrían estar causando la ausencia de la producción de espermatozoides. En la mayoría de los casos, las pruebas genéticas no revelan la causa de la ausencia de la producción de espermatozoides. Sin embargo, es fundamental realizarlas.
Los hombres con un bloqueo de espermatogénesis tienen que someterse a una intervención con el fin de intentar encontrar espermatozoides para la fecundación de un óvulo a través de FIV/ICSI, ya que los espermatozoides extraídos del testículo no han aprendido a nadar todavía, a pesar de ser perfectamente capaces de concebir un bebé a través de FIV/ICSI. Un reciente estudio demográfico publicado en 2016 por Cissen et al. indica que solo un 43,7% de hombres con un bloqueo de espermatogénesis tuvieron éxito en el procedimiento inicial de la Extracción Testicular de Espermatozoides (TESE), definido por la presencia de espermatozoides en la muestra quirúrgica (3). De manera similar, otro estudio retrospectivo demográfico publicado por Vloeberghs et al. en 2015, muestra que la tasa de éxito de la recuperación de espermatozoides durante la primera TESE es de solo un 40,5% entre los hombres con un bloqueo de espermatogénesis (4). A pesar de los porcentajes de éxito de la recuperación de espermatozoides con TESE, finalmente sólo una pequeña minoría de los pacientes con un bloqueo de espermatogénesis se convierten en padres biológicos. Entre los 714 varones con un bloqueo de espermatogénesis sometiéndose a TESE, sólo uno de cada siete hombres (13,4%) procreó un hijo biológico finalmente (4). Otras publicaciones señalaron una tasa de éxito un poco más prometedora gracias a un método de la Extracción Testicular de Espermatozoides con amplificación visual microscópica (micro-TESE), realizado en casos de un bloqueo de espermatogénesis, con espermatozoides aislados en aproximadamente un 60% de las muestras quirúrgicas (5). MicroTESE encuentra espermatozoides en aproximadamente un 40-60% de los casos en nuestra clínica IVIRMANJ. Desgraciadamente, hasta hace poco los hombres no tenían otras opciones de tener hijos biológicos si no se encontraban espermatozoides al realizar microTESE. Por lo tanto, muchos hombres no disponen de espermatozoides maduros que se puedan aislar con éxito, incluso con la ayuda de intervenciones quirúrgicas de extracción de espermatozoides.
Sin embargo, se ha sugerido que las espermátidas redondas, los precursores inmaduros de espermatozoides maduros, se pueden inyectar en ovocitos humanos con éxito y, por lo tanto, se pueden emplear en vez de espermatozoides maduros como último recurso (4, 5). Entre los hombres con un bloqueo de espermatogénesis en el caso de cuales no se pudieron aislar de la muestra testicular ni espermatozoides maduros ni espermátidas de una fase avanzada, en un 30% de pacientes sí se encontraron espermátidas redondas en las muestras quirúrgicas (6). Tanto en los modelos animales como de humanos se han producido nacimientos gracias al uso de la técnica de Inyección Intracitoplasmática de Espermátidas Redondas (ROSI). Aunque los primeros informes describían ROSI como ineficaz y sin ningún valor para el uso clínico, los estudios recientes la declaran una alternativa viable para pacientes que se niegan a la donación de semen. Es importante que ROSI parece dar como resultado hijos sin problemas atípicos físicos, mentales o epigenéticos (4,5). La publicación más reciente de Tanaka et. al en 2018 reportó 90 niños nacidos como resultado de ROSI e investigó y monitoreó durante dos años su desarrollo físico y cognitivo. No se observaron diferencias importantes entre los hijos nacidos a través de ROSI en comparación con concepciones espontáneas durante el tiempo de observación de dos años (5).
Como un investigador clínico y quirúrgico de ciencias aplicables, una de las conversaciones más difíciles que tengo con los pacientes es cuando les digo que no se encontraron espermatozoides por medio de microTESE, ya que hasta ahora, no había ninguna otra manera de ayudar a esos hombres a tener sus propios hijos biológicos. Hasta la publicación del informe más reciente, demostrando que 90 bebés nacieron mediante ROSI, fui muy escéptico de este método y no lo quería recomendar a pacientes. Actualmente, no hay ningún laboratorio en Estados Unidos que suela emplear ROSI para FIV en varones cuando no presentan espermatozoides mediante microTESE. La idea de empezar un ensayo clínico en IVIRMANJ ha despertado mi interés recientemente, con el fin de ofrecer este tratamiento a pacientes en búsqueda de cura para la infertilidad masculina, que se sometieron a microTESE y no presentaron espermatozoides viables a la hora de la cirugía.
Uno de los problemas principales de ROSI consiste en que las espermátidas redondas obtenidas de hombres con un fallo de espermatogénesis a través de microTESE, frecuentemente no fecundan el óvulo muy bien. Cuando logran fecundar un óvulo, son perfectamente capaces de concebir un bebé sano, pero parecen fecundar óvulos a una tasa significativamente menor que los espermatozoides completamente maduros procedentes del testículo. En IVIRMANJ tenemos acceso a uno de los microscopios confocales más potentes del mundo, capaz de visualizar tejido testicular humano con muy alta resolución tras marcarlo con sondas moleculares codificadas con colores. Nuestra sospecha es que la población de espermátidas redondas realmente capaces de fecundar un óvulo puede ser muy pequeña. Esperamos que este microscopio pronto nos permitirá identificar esa población de espermátidas, favoreciendo la tasa de fecundación y llevando a que más niños nazcan con la ayuda de esta técnica. Estamos actualmente en el proceso de poner en marcha el ensayo clínico con deseando que suba la tasa de éxito del tratamiento y que podamos ofrecer esperanza a los hombres en los que no se encuentran espermatozoides a través de microTESE. Nuestra ambición es lograr encontrar la manera de tratar esta afección devastadora y ofrecer esperanza a los hombres tras fracasar todas las demás formas de tratamiento.
Post by James Hotaling, M.D.
Referencias:
- Stephen EH, Chandra A. Declining estimates of infertility in the United States: 1982-2002. Fertility and sterility. 2006;86(3):516-23. Epub 2006/09/06. doi: 10.1016/j.fertnstert.2006.02.129. PubMed PMID: 16952500.
- Levine H, Jorgensen N, Martino-Andrade A, Mendiola J, Weksler-Derri D, Mindlis I, Pinotti R, Swan SH. Temporal trends in sperm count: a systematic review and meta-regression analysis. Hum Reprod Update. 2017;23(6):646-59. doi: 10.1093/humupd/dmx022. PubMed PMID: 28981654.
- Thoma ME, McLain AC, Louis JF, King RB, Trumble AC, Sundaram R, Buck Louis GM. Prevalence of infertility in the United States as estimated by the current duration approach and a traditional constructed approach. Fertil Steril. 2013;99(5):1324-31.e1. Epub 2013/01/08. doi: 10.1016/j.fertnstert.2012.11.037. PubMed PMID: 23290741; PMCID: Pmc3615032.
- A Tanaka MN, Y Takemoto, I Tanaka, H Kusonoki, S Watanabe, K Kuroda, S Takeda, M Ito, R Yanagimachi. Fourteen babies born after round spermatid injection into human oocytes. Proc Natl Acad Sci USA. 2015;112(47):14629-34.
- A Tanaka KS, M Nagayoshi, A Tanaka, Y Takemoto, S Watanabe, S Takeda, M Irahara, N Kuji, Z Yamagata, R Yanagimachi. Ninety babies born after round spermatid injection into oocytes: survey of their development from fertilization to 2 years of age. Fertil Steril. 2018;110(3):443-51.
- A Tanaka IT, M Nagayoshi, S Awata, N Himeno, H Kusunoki. In vitro culture of the immature spermatogenic cells. Fertil Steril. 2006;86(3):Suppl S518-S9.