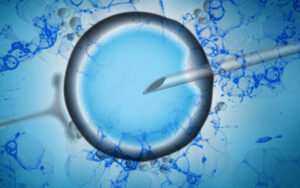
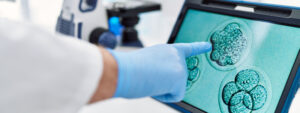
Se cree que el mosaicismo embrionario, definido como la presencia de más de una línea de células diferentes desde el punto de vista del cariotipo, se produce casi exclusivamente como resultado de un error de no disyunción meiótica en el embrión postcigótico. La aparición de la tecnología de secuenciación masiva (NGS, por sus siglas en inglés) para la realización del diagnóstico genético preimplantacional de aneuploidías (PGT-A, por sus siglas en inglés) ha permitido un diagnóstico más preciso de la aneuploidía embrionaria, pero también ha aumentado el número de mosaicismos detectados debido a la mayor profundidad y resolución del método de amplificación y detección. Cabe destacar que el único fin del PGT-A es detectar aneuploidías, no la presencia de mosaicismo. La presencia de mosaicismo dentro del blastocisto es mucho mayor a la detectada dentro de la biopsia, compuesta por 5-10 células de trofoblastos. Además, un resultado PGT-A mosaico no concluye la presencia de mosaicismo en la masa celular interna (ICM, por sus siglas en inglés).
Muchas de las plataformas PGT-A disponibles comercialmente se basan en la amplificación de genoma entero (WGA, por sus siglas en inglés), seguida del “agrupamiento” de amplicones, lo que permite generar un número de copias de cromosomas individuales. Una de las cuestiones inherentes a este método es lo limitado de cada una de las lecturas, lo que disminuye la exactitud de la interpretación del genotipo. Este tipo de plataformas diagnostica un embrión como mosaico si el porcentaje de células aneuploides se encuentra entre el 20 y el 80%, con menos del 20% se etiquetan como euploides y con más del 80% como aneuploides. Algunas plataformas distinguen también “mosaicos de nivel reducido”, con el 20-40% de aneuploides, y “mosaicos de nivel elevado”, con el 40-80% del ADN aneuploide. La amplitud de este espectro tiende a aumentar el diagnóstico de embriones como mosaicos y a sobrestimar o subestimar su verdadera capacidad de desarrollar un bebé sano. Asimismo, aunque se estima que las muestras de biopsia contienen entre 5 y 10 células de trofoblastos, la cantidad de ADN incluido en la muestra no puede cuantificarse con exactitud, hecho que pone la validez de estos umbrales en entredicho. La confianza en los números de copias de cromosomas y los porcentajes log2 intermedios estimados, o el porcentaje de contenido de ADN relativo por cromosoma puede llevar a falsos positivos en el diagnóstico de embriones como mosaicos.
En IVIRMA se ha desarrollado una innovadora plataforma PGT-A que se basa en una amplificación previa dirigida, esta proporciona una mayor profundidad en la cobertura mediante el análisis de una serie de copias y la genotipificación simultánea de polimorfismos de nucleótido único (SNP, por sus siglas en inglés). Esto impide la clasificación de los embriones como mosaicos basándose únicamente en la variación del número de copias. La NGS dirigida (tNGS, por sus siglas en inglés) ha demostrado que embriones que, en un primer momento, se consideraban mosaicos basándose en un porcentaje log2 modificado, son en realidad euploides, aneuploides o poliploides. Una mayor profundidad de cobertura en cada locus aumenta la exactitud genotípica. Se estima que la poliploidía, que a menudo se confunde con mosaicismo en algunas plataformas comerciales basadas en WGA, es la causa del 2% de las pérdidas de embriones y del 15% de embarazos citogenéticamente anormales (1). Una única muestra de biopsia es suficiente para el cribado de aneuploidías, la detección de mosaicismo y el diagnóstico de trastornos monogenéticos. La incidencia del mosaicismo al utilizar la plataforma tNGS de IVIRMA es del 3-4% en los blastocistos de implantación previa.
El diagnóstico del mosaicismo ha enfrentado a desafíos a la comunidad de la tecnología de reproducción asistida (TRA), ya que se ha constatado que poseen un menor potencial reproductivo que los embriones euploides (2). En los últimos años, se ha planteado la hipótesis de que los embriones mosaicos podrían culminar en nacimientos de bebés sanos aunque exista un solapamiento entre los niveles de disomía y mosaico para el diagnóstico de NGS, pero las consecuencias a largo plazo para la salud de los individuos todavía se desconocen (3). En IVIRMA se está llevando a cabo un estudio no selectivo en los que los embriones se transfieren a ciegas a los resultados de PGT-A, esto aportaría la prueba definitiva del verdadero potencial reproductivo de los blastocistos mosaicos.
Para parejas con una cohorte de embriones limitada para la criopreservación, los determinados como mosaicos pueden ser contraproducentes para sus objetivos de formar una familia ya que no existe una evidencia suficiente de transferencia rutinaria. La transferencia de embriones mosaico solo es aceptable si no hay embriones considerados euploides tras PGT-A, o si la cantidad de embriones euploides se ha agotado. Las directrices de la Sociedad Internacional de Diagnóstico Genético Preimplantacional (PGDIS, por sus siglas en inglés), aunque se apoyan en datos limitados, sugieren que se debe dar prioridad a la transferencia de embriones basada en los niveles de mosaicismo así como en el número y los cromosomas específicos implicados (4). Los embriones mosaico diploides-aneuploides con los cromosomas 13, 15, 16, 18, 21, 22, X e Y afectados se consideran de “alto riesgo” dado su posible conexión con la isodisomía uniparental, una restricción grave del crecimiento intrauterino y la posibilidad de un nacimiento vivo aneuploide. De manera similar, se ha sugerido que la transferencia de monosomías-euploides deberían priorizarse frente a las trisomías-euploides debido al reducido potencial reproductivo de las primeras. Sin embargo, se podría pensar que si hay monosomías, es probable que haya una trisomía recíproca en el embrión. Debido a lo reducido de las pruebas, no resulta inaceptable transferir estos embriones de alto riesgo, pero únicamente si no existen alternativas mosaicas de “bajo riesgo”. La ausencia de alternativas más adecuadas para la transferencia es indudablemente excepcional. Se han realizado innumerables avances en la optimización de las plataformas PGT-A como evidencian clínicamente los incrementos de transferencias de embrión único, dando lugar a una tasa mayor de nacimientos vivos y una tasa menor de abortos espontáneos así como una reducción de la morbilidad obstétrica y neonatal asociada con los embarazos por fecundación in vitro. A medida que realizamos un cultivo postimplantación de blastocitos mosaicos más amplio aprendemos muchísimo más sobre la ciencia básica en torno a estos embriones. Básicamente, la misión de IVIRMA es usar estrategias innovadoras para desarrollar y perfeccionar nuevas tecnologías para optimizar los resultados y aumentar la disponibilidad de PGT-A para pacientes de todo el mundo.
Author: Richard T Scott