Recuperar la fertilidad de la mujer mediante la bioingeniería.
El trasplante de órganos es actualmente un hecho bastante común en la práctica médica habitual. Sin embargo, la creciente demanda ha provocado una larga lista de espera para este tipo de pacientes, y generalmente no se dispone de suficiente suministro para abastecer toda esta demanda. Algunas de estas necesidades han sido cubiertas gracias a las nuevas tecnologías biomédicas, que permiten la sustitución de determinados órganos y su control mediante unos dispositivos específicos. En ciertos casos (por ejemplo en el corazón mediante dispositivos tales como sensores, válvulas etc..) estos han sido efectivos incluso en personas que han perdido completamente la función del órgano, debido a una enfermedad o lesión, y han podido al menos parcialmente, recuperar la función original. Pese al éxito de estas nuevas realidades, es necesario continuar investigando para superar desafíos tales como la disponibilidad de órganos y el rechazo de tejidos.
Cuando los órganos (bio)artificiales se convierten en una realidad
Existen recientes investigaciones sobre nuevas alternativas que pueden evitar posibles complicaciones relacionadas tanto con los órganos trasplantados como con las nuevas tecnologías biomédicas: los órganos (bio)artificiales. Estas nuevas alternativas están creadas en el laboratorio con el uso de la bioingeniería y estrategias de medicina regenerativa y pretenden la reconstrucción/reparación/sustitución de órganos y/o tejidos. Aunque las aproximaciones metodológicas son muy diversas, todas implican el uso de material de ‘andamiaje’ o (bio)moldes que dan soporte a las células y permiten el crecimiento y desarrollo de los tejidos (Costa et al., 2017). Estos andamios o (bio)moldes pueden ser construidos en el laboratorio mediante el desarrollo de sistemas tri-dimensionales (3D) (por ejemplo, uso de materiales sintéticos o bio-impresoras), o pueden estar basados en procedimientos de descelularización de órganos, proceso mediante el cual las células son eliminadas de los órganos naturales manteniendo la estructura tridimensional original (biomoldes) (Dzobo et al., 2018). Otra novedad reciente incluye los ‘órganos en un chip’ (del inglés “organs-on-a-chip”), un dispositivo que recrea a micro-escala las funciones e interacciones vitales de determinados órganos (Sosa-Hernández et al., 2018). Finalmente, el cultivo celular in vitro 3-D ha permitido la creación de organoides, cuyo resultado es una versión miniaturizada de los órganos nativos, con estructura y organización idénticas a los órganos originales (Artegiani et al., 2018). Estas nuevas alternativas pueden permitir avances muy relevantes en el área del trasplante de órganos, así como en su regeneración, restauración y recuperación.
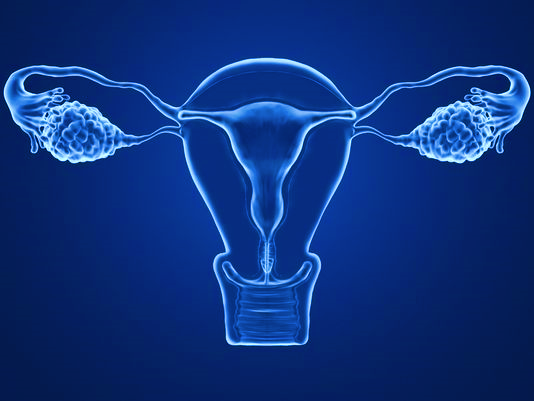
Bioingeniería del aparato reproductor femenino
Estos nuevos enfoques se han desarrollado gracias a la bioingeniería, un prometedor y creciente campo de investigación en medicina regenerativa que pretende transformar la medicina traslacional. La bioingeniería también puede aplicarse en medicina reproductiva, ya que puede tratar de resolver diversas patologías y anomalías que pueden dar lugar a infertilidad femenina (Campo et al., 2017). Por ejemplo, uno de los casos que refleja los avances de la bioingeniería uterina fue un estudio de 2014 que demostró con éxito la creación ex vivo de tejidos vaginales (constructos neo-vaginales) y su implantación en pacientes con aplasia vaginal (Raya-Rivera et al., 2014).
Sin embargo, a pesar de estos avances, todavía existen algunas mujeres diagnosticadas con patologías que afectan directamente al útero o los ovarios y, en consecuencia, a la fertilidad. Entre estas patologías se incluyen la infertilidad absoluta de origen uterino (AUFI), el cáncer de ovario, el síndrome del ovario poliquístico, la endometriosis y el fallo ovárico precoz, entre otros (Hewlett y Mahalingaiah, 2015; Qin et al., 2015). Emplear la bioingeniería para tratar de recuperar/reparar el aparato reproductor femenino puede ofrecer opciones reales de tratamiento para este tipo de patologías, y por lo tanto recuperar la fertilidad de estas mujeres.
El futuro próximo: crear ovarios e hidrogeles ováricos
Técnicas como la impresión 3-D y la ingeniería de órganos/tejidos suponen un camino prometedor para la creación de ovarios bio-artificiales (Amorim et al., 2016). Varios equipos de investigación han desarrollado ovarios artificiales trasplantables, usando polímeros artificiales como matriz, o usando biomoldes derivados de órganos descelularizados. El objetivo principal es mimetizar el micro-entorno o nicho del ovario natural. Además, estudios innovadores que implican el desarrollo de los “organs-on-a-chip” (“tissue papers”) y los organoides en 3-D también han sido empleados en el campo de la reproducción (Jakus et al., 2017; Campo et al., 2017). Pero, pese a estos grandes avances, se sigue necesitando más investigación para conseguir (bio)moldes ováricos trasplantables competentes que sean exitosos en nuestras pacientes.
Uno de los objetivos principales es activar la producción de ovocitos maduros en mujeres con infertilidad de origen ovárico. En la última década, la foliculogénesis in vitro ha experimentado adelantos exponenciales. Varias investigaciones biomédicas han logrado desarrollar in vitro folículos en un entorno 3-D. Sin embargo, los biomateriales usados para ello son hidrogeles no específicos (alginato, colágeno y fibrina) que presentan algunas limitaciones, tales como no activar las interacciones con las células encapsuladas. Por ello, en la actualidad se están proponiendo los hidrogeles con origen biológico de matriz extracelular (MEC) desde diferentes órganos y tejidos. Estos hidrogeles únicos son creados a partir de órganos descelularizados y han sido empleados con éxito en diferentes órganos y tejidos con fines regenerativos porque proporcionan un entorno 3-D específico casi idéntico al original. La tendencia más reciente de la bioingeniería ovárica está basada en el uso de hidrogeles de MEC proveniente de ovarios descelularizados, aportando por primera vez los primeros pasos para el desarrollo y estudio de la foliculogénesis in vitro (Laronda et al., 2015; Liu et al., 2017). Los protocolos de descelularización de ovarios descritos están basados en el uso del detergente SDS, sodio dodecyl sulfato, que provoca la separación o lisado celular necesario para la obtención del biomolde; sin embargo, este detergente tiene algunos efectos adversos.
En el área de innovación de IVIRMA, nuestro grupo de investigación ha realizado experimentos preliminares en ovarios con un detergente diferente al descrito hasta la fecha, el sodio deoxicolato (SDC), que es generalmente considerado menos lesivo que el comúnmente usado SDS. Nuestros resultados iniciales han sido bastante prometedores ya que el examen microscópico de los ovarios tratados con SDC demostró la ausencia de núcleos y, por tanto, la eficiente eliminación de ADN. Al mismo tiempo, la estructura o biomolde 3-D del tejido ovárico se conservó después del tratamiento de descelularización. Nuestro próximo objetivo será ampliar este trabajo creando un sistema de cultivo in vitro en 3-D basado en el uso de hidrogeles de MEC desde los ovarios descelularizados, y así recrear la funciones biológicas propias del órgano.
Para concluir, destacar que varios estudios de investigación están obteniendo resultados prometedores como el restablecimiento de la fertilidad ovárica mediante la generación de (bio)moldes trasplantables y/o el desarrollo de hidrogeles de origen ovárico que imitan el micro-ambiente ideal para el desarrollo de la foliculogénesis in vitro.
Post de Dra. Irene Cervelló
Manager del Laboratorio de la Fundación IVI e Investigadora Principal del grupo de investigación de Células Madre Endometriales y Bioingeniería.
References:
- Amorim CA, Shikanov A. The artificial ovary: current status and future perspectives. Future Oncol. 2016 Oct;12(20):2323-32.
- Artegiani B, Clevers H. Use and application of 3D-organoid technology. Hum Mol Genet. 2018 Aug 1;27(R2):R99-R107.
- Costa A, Naranjo JD, Londono R, Badylak SF. Biologic Scaffolds. Cold Spring Harb Perspect Med. 2017 Sep 1;7(9).
- Dzobo K, Thomford NE, Senthebane DA, Shipanga H, Rowe A, Dandara C, Pillay M, Motaung KSCM. Advances in Regenerative Medicine and Tissue Engineering: Innovation and Transformation of Medicine. Stem Cells Int. 2018 Jul 30;2018:2495848.
- Hewlett M, Mahalingaiah S. Update on primary ovarian insufficiency. Curr Opin Endocrinol Diabetes Obes. 2015 Dec;22(6):483-9.
- Jakus AE, Laronda MM, Rashedi AS, Robinson CM, Lee C, Jordan SW, Orwig KE, Woodruff TK, Shah RN. «Tissue Papers» from Organ-Specific Decellularized Extracellular Matrices. Adv Funct Mater. 2017 Sep 13;27(3).
- Liu WY, Lin SG, Zhuo RY, Xie YY, Pan W, Lin XF, Shen FX. Xenogeneic Decellularized Scaffold: A Novel Platform for Ovary Regeneration. Tissue Eng Part C Methods. 2017 Feb;23(2):61-71.
- Qin Y, Jiao X, Simpson JL, Chen ZJ. Genetics of primary ovarian insufficiency: new developments and opportunities. Hum Reprod Update. 2015 Nov-Dec;21(6):787-808.
- Raya-Rivera A. M, Esquiliano D, Fierro-Pastrana R, López-Bayghen E, Valencia P, Ordorica-Flores R, Soker S, Yoo J. J, and Atala A. Tissue-engineered autologous vaginal organs in patients: a pilot cohort study. Lancet 384:329–336, 2014.
- Sosa-Hernández JE, Villalba-Rodríguez AM, Romero-Castillo KD, Aguilar-Aguila-Isaías MA, García-Reyes IE, Hernández-Antonio A, Ahmed I, Sharma A, Parra-Saldívar R, Iqbal HMN. Organs-on-a-Chip Module: A Review from the Development and Applications Perspective. Micromachines (Basel). 2018 Oct 22;9(10).